O QUE VOCÊ
PRECISA?

Comitê de Ética em Pesquisa
O Comitê de Ética em Pesquisa (CEP) do Hospital Geral de Fortaleza (HGF) é um órgão institucional, colegiado, interdisciplinar e independente, de caráter consultivo, deliberativo e educativo, com vinculação institucional à Superintendência da unidade, tendo sua aprovação e credenciamento na Comissão Nacional de Ética em Pesquisa (CONEP), do Conselho Nacional de Saúde (CNS) do Ministério da Saúde, por meio da carta nº399 CNS/CONEP.
O CEP do HGF tem como principal missão a defesa dos interesses dos participantes da pesquisa em sua integridade e dignidade, além de contribuir para qualidade das pesquisas, primando para que estas ocorram dentro de padrões éticos, de acordo com a Resolução 466/12, do CNS.
Membros
Coordenadora:
– Patrícia Quirino Costa – Farmacêutica – Doutora
Coordenadora Adjunta:
– Adna Ribeiro Braquehais – Enfermeira – Mestra
Membros Efetivos:
– Jane Eyre Rodrigues Azevedo – Psicóloga – Mestra
– Fred Ribeiro Santiago – Fisioterapeuta – Mestre
– Luísa Maria Oliveira Pinto – Nutricionista – Mestra
– Yuri Fontenelle Lima Montenegro – Terapeuta Ocupacional – Mestre
– Sarah Suyanne Carvalho Melgaço – Médica – Mestra
– Francisco Oberlando Nascimento Mendonça (Léo Girão) – Representante dos Participantes de Pesquisa
Suplentes
– Ondina Maria Chagas Canuto – Assistente social – Doutora
– Maria Lurdete Nascimento de Souza – Representante dos Participantes de Pesquisa
– Simone Oliveira Lucas Bertoldo – Enfermeira – Mestra
Secretaria executiva
– Mônica Medeiros de Vasconcelos – Enfermeira – Mestra
Horário de atendimento
Segundas-feiras, das 7h às 11h
Terças-feiras, das 7h às 16h
Quartas-feiras, das 7h às 16h
Quintas-feiras, das 7h às 11h
Calendário de reuniões
As reuniões ordinárias do CEP do HGF ocorrem mensalmente, quando são discutidos os projetos submetidos, relatos de eventos adversos e outros assuntos relacionados à ética envolvida na condução de projetos de pesquisa com seres humanos, conforme calendário abaixo.
Baixe o calendário de reuniões do CEP em 2026 aqui.
Fluxo regulatório de pesquisa no HGF
O fluxo regulatório para submissão de projetos de pesquisa no CEP/HGF exige que os projetos que se pretende realizar nesta instituição, devam seguir as etapas descritas a seguir:
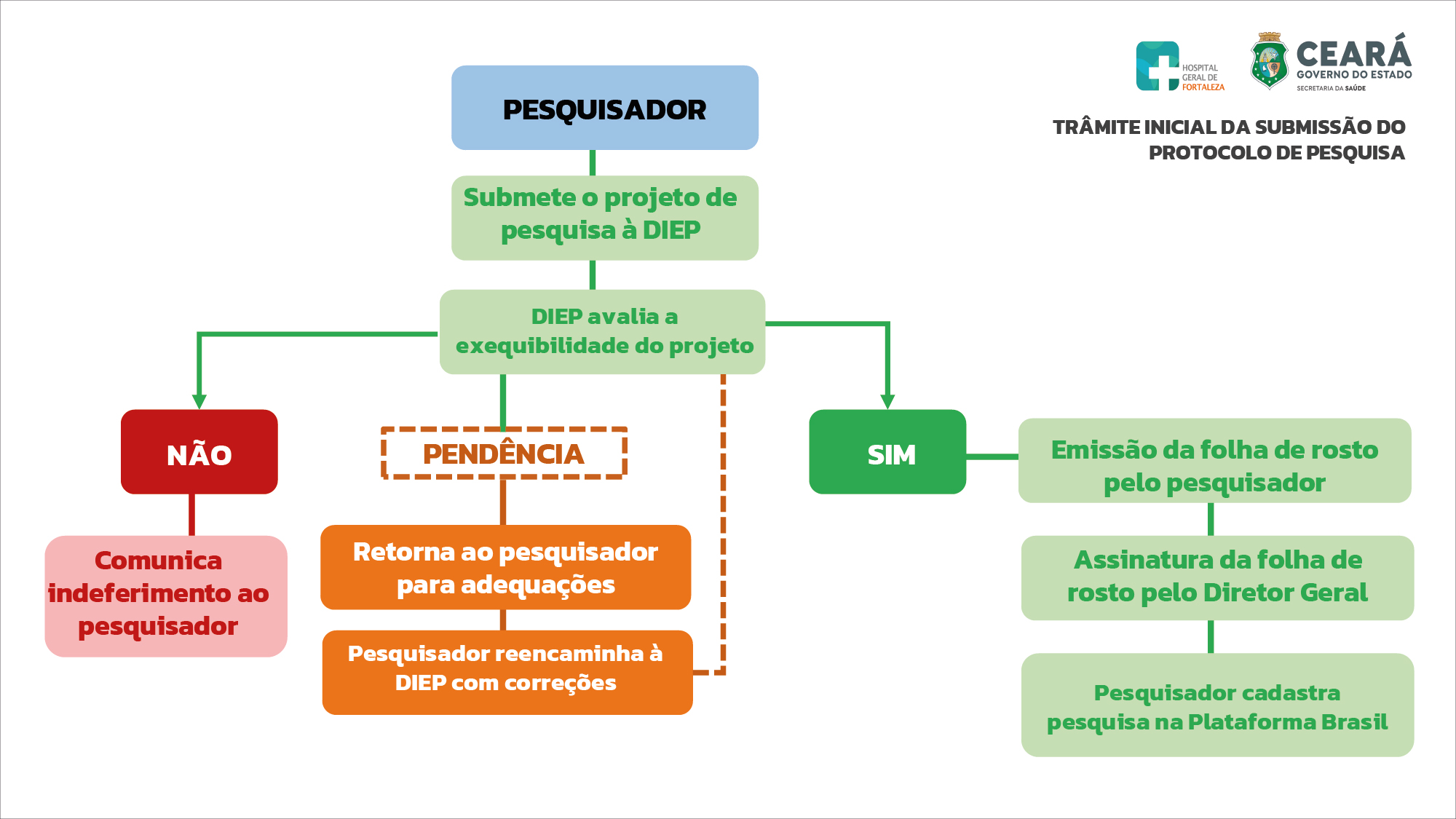
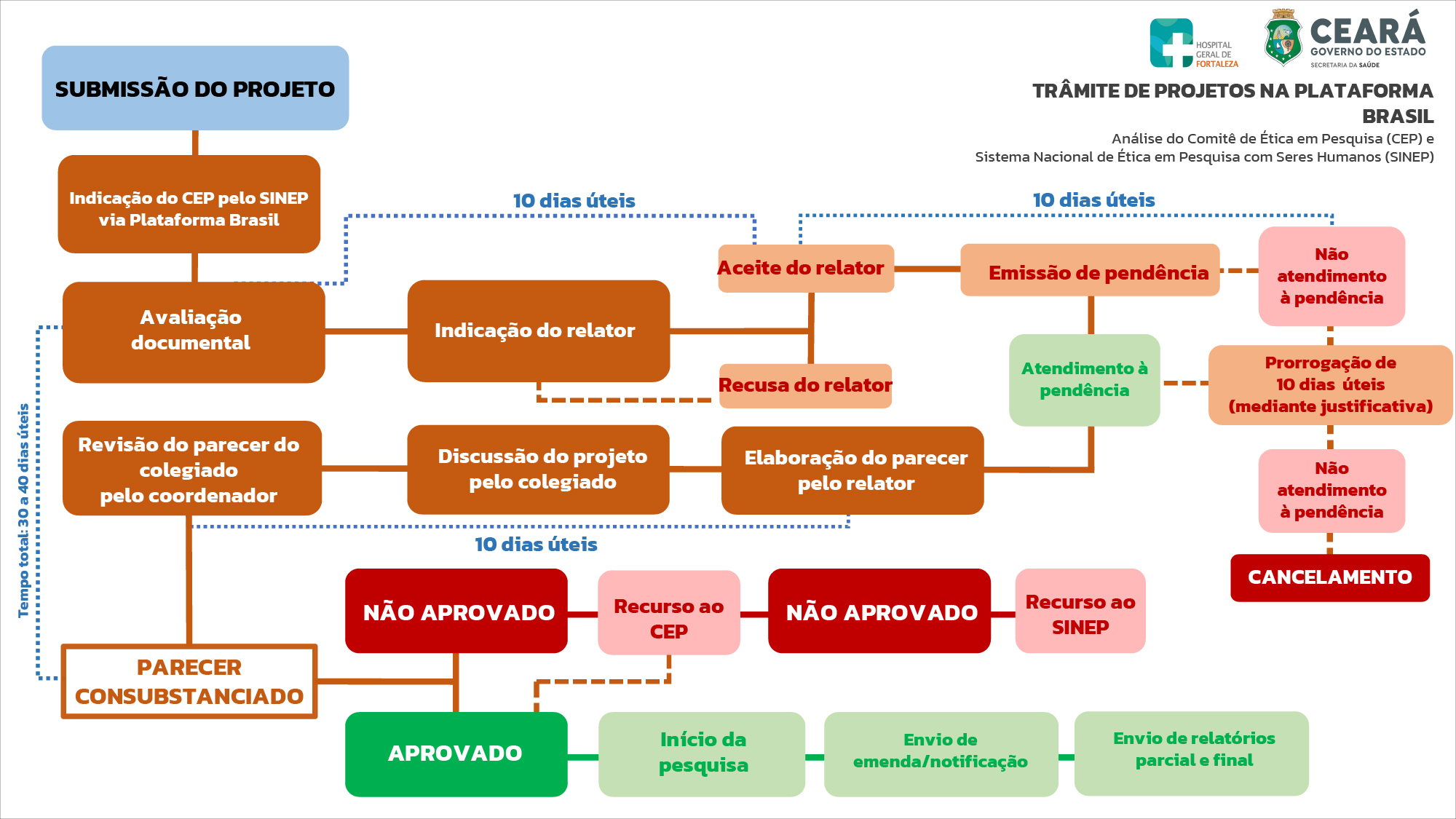
Imagem: Análise e Tramitação de Projetos nos Comitês de Ética em Pesquisa, versão 4.1 – pág.3.
Regimento Interno
– Baixe o Regimento Interno do CEP aqui.
– Para acessar a Plataforma Brasil, clique aqui.
Legislações
– Resolução 466/12 do CNS – Diretrizes e normas para pesquisas envolvendo seres humanos.
– Resolução 510/16 do CNS – Resolução complementar à Resolução 466/12 e trata de pesquisas em Ciências Humanas e Sociais.
– Resolução 411/11 do CNS – Pesquisas envolvendo material biológico humano.
– Resolução 728/24 do CNS -Dispõe sobre o uso de bancos de dados com finalidade de pesquisa científica envolvendo seres humanos.
– Norma Operacional N°001/2013 do CNS – Fornece procedimentos para submissão, avaliação e acompanhamento da pesquisa e de desenvolvimento envolvendo seres humanos no Brasil.
– Carta Circular 013/2020 do CNS – Tramitação de Eventos Adversos no Sistema CEP/Conep.
– Carta Circular 166/2018 do CNS – Tramitação de Relatos de Casos.
– Carta Circular 039/2011 do CNS – Uso de dados de prontuários para fins de pesquisa.
– Resolução 346/05 do CNS – Projetos de pesquisa multicêntricos.
– Resolução 340/04 do CNS – Área temática especial: pesquisa em genética humana.
– Resolução 292/99 do CNS – Área temática especial: pesquisas coordenadas do exterior ou com participação estrangeira e pesquisas que envolvam remessa de material biológico para o exterior.
– Resolução 251/97 do CNS – Pesquisa com novos fármacos, medicamentos, vacinas e testes diagnósticos.
– Lei nº 14.874/24 – Dispõe sobre a pesquisa com seres humanos e institui o Sistema Nacional de Ética em Pesquisa com Seres Humanos.
– Decreto nº 12.651/25 – Regulamenta a Lei nº 14.874, de 28 de maio de 2024, que dispõe sobre a pesquisa com seres humanos e institui o Sistema Nacional de Ética em Pesquisa com Seres Humanos.
– Nota Técnica Nº 43/2025 – DECIT/SECTICS/MS – Orientações sobre a tramitação e a classificação de risco de pesquisas no âmbito do Sistema Nacional de Ética em Pesquisa com Seres Humanos (SINEP).
– Ofício nº 183/2024/CONEP/SECNS/DGIP/SE/
NOTA TÉCNICA No 1_2026_DECIT_SCTIE_MS – Nota Técnica Nº 1/2026-DECIT/SCTIE/MS
Orientações diversas
Neste espaço, você pode conferir orientações diversas do Comitê de Ética em Pesquisa do HGF para realização de pesquisas. Aguarde mais orientações em breve.
– Manual de Pendências Recorrentes
– Orientações para submissão de projeto de pesquisa
– Orientações para Pesquisas em Ambiente Virtual
– Template de projeto HGF
– Cartilha dos Direitos dos Participantes de Pesquisa
– Notificação Modelo Envio de Relatório Parcial
– Notificação Modelo Envio de Relatório Final
– Roteiro para elaboração de Relatório Final
– Roteiro para elaboração de Relatório Parcial
– Passo a passo para envio de Notificações no sistema CEP/CONEP
– Passo a passo para envio de Emendas no sistema CEP/CONEP
Dúvidas frequentes
1. Como dever ser efetuada a submissão de projetos de pesquisa no HGF?
O pesquisador deverá inicialmente enviar o arquivo do Projeto e da documentação obrigatória para o e – mail (pesquisaclinica.hgf@gmail.com) da Coordenação da Direção de Ensino, Pesquisa e Residência (DIEP/HGF). Nesta Coordenação, o projeto seja avaliado e após aprovação, será liberada uma carta de aprovação para o desenvolvimento do projeto no hospital e recomendação para assinatura da folha de rosto pelo Diretor Geral do HGF, caso o hospital seja a instiuição proponente.
2. Quais documentos devem ser inseridos obrigatoriamente na plataforma Brasil para submissão do projeto ao CEP?
Ao submeter o projeto na Plataforma Brasil, deverão ser anexados os seguintes documentos obrigatórios:
– Folha de Rosto – assinada pelo pesquisador e pelo Diretor Geral do HGF ou da Instituição à qual o projeto está vinculado
– Projeto Original Completo
– Declaração de Compromisso de Pesquisador(a)
– Declaração de Concordância dos Pesquisadores Envolvidos no estudo
– Termo de Fiel Depositário
– Termo de Ciência e Colaboração para Participação em Pesquisa Realizada no HGF
– Termo de Anuência e Viabilidade para Pesquisa com uso de Telemedicina
– Autorização do Chefe do Serviço (Carta de Anuência)
– Carta de Anuência do Núcleo de Atendimento ao Cliente – NAC/HGF
– Declaração de Instituição e Infraestrutura – necessária para o desenvolvimento da pesquisa no caso de entrevistas ou grupos focais, assim como para atender eventuais problemas dela resultante. A declaração deve expressar a concordância da instituição
– Declaração de Manuseio de Material Biológico/Biorrepositório/Biobanco
– Acordo entre as Instituições Envolvidas no Armazenamento e Análise de Amostras Biológicas em Biorrepositório
– Instrumento de Coleta de Dados – questões norteadoras, questionários, roteiros de entrevistas, etc.
– Termo de Consentimento Livre e Esclarecido (TCLE) – somente para pesquisas com participantes maiores de 18 anos de idade
– Termo de Consentimento Livre e Esclarecido (TCLE) – Pais ou Responsáveis – somente para pesquisas com participantes menores de 18 anos
– Termo de Consentimento Livre e Esclarecido (TCLE) de banco de material biológico humano
– Termo de Assentimento Livre e Esclarecido (TALE) – somente para pesquisas com participantes com idade entre 7 a 17 anos de idade
– Termo de Autorização de uso de Imagem e Voz e Respectiva Cessão de Direitos
– Termo de Ciência do Pesquisador Sobre a Comunicação ao Ministério Público
– Modelo de Orçamento (detalhar os recursos, fontes e destinação) e Cronograma (com datas atualizadas, descrevendo a duração total e as diferentes etapas da pesquisa, de início da coleta de dados posterior à aprovação do CEP/HGF)
– Checklist para Relato de Caso
– Checklist para Outros Tipos de Pesquisa
– Modelo de carta-resposta
Observar o alinhamento de informações nos diferentes anexos.
3. Quais os principais pontos de atenção?
– Toda pesquisa tem riscos, logo faz-se necessário descrever detalhadamente os riscos e benefícios da pesquisa (projeto detalhado, projeto original completo e TCLE), assim como os cuidados e providências necessárias para minimizar os riscos.
– As cartas de anuência do NAC e dos chefes dos setores devem vir com o período de coleta descrito.
4. Até quando posso inserir projetos e responder pendências?
Mínimo 10 dias de antecedência das reuniões descritas no calendário.
5. Monitoramento dos protocolos analisados pelo CEP HGF
– Projetos, emendas e notificações avaliadas
6. Em caso de dúvida, como proceder?
Comparecer ao CEP HGF, enviar e- mail para cephgf.ce@gmail.com ou ligar para (85) 3106-3891 ou 3892.
